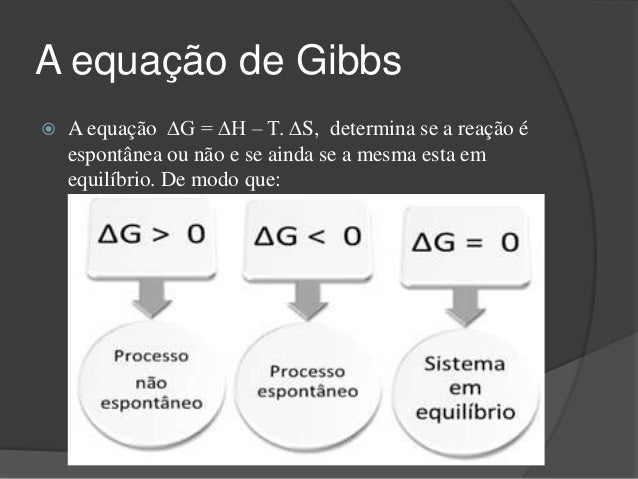
Entenda entropia e saiba quando uma reação será ou não espontânea. Area VIP) Link para aquisição dos. A variação de energia de uma transformação que é utilizável ou disponível para realizar um trabalho, damos o nome de variação de energia livre (∆G). Imagine, por exemplo, uma reação que libera calor ( energia ). Unidades da energia livre de Gibbs. A mudança de energia livre de Gibbs (Δ G) e como ela está relacionada com equilíbrio e espontaneidade da reação.
Se você está vendo esta mensagem, significa que estamos tendo problemas para carregar recursos externos em nosso website. Visto que em um processo a energia nunca é totalmente convertida em trabalho, a fração de energia útil do sistema, isto é, que realiza o trabalho, é considerada a energia livre. A parcela de energia interna F que pode ser convertida em trabalho, assim como a entropia , é uma função de estado do sistema, e por tal dá origem a um potencial termodinâmico: a energia livre de Helmholtz do sistema em consideração.
Em se tratando de energia livre e de entropia , analise as seguintes proposições: I. A energia livre pode ser positiva ou negativa, mas nunca pode ser nula. Não são espontâneos os processos que ocorrem com aumento de entalpia e diminuição de entropia. Gibbs é uma função da entalpia e da entropia. Entendendo a entropia De acordo com a segunda lei da termodinâmica, o trabalho pode ser totalmente convertido em calor e em seguida em energia térmica, mas essa última, jamais poderá ser completamente convertida em trabalho. O objetivo desse cientista era propor uma forma mais certa de determinar a espontaneidade de um processo.
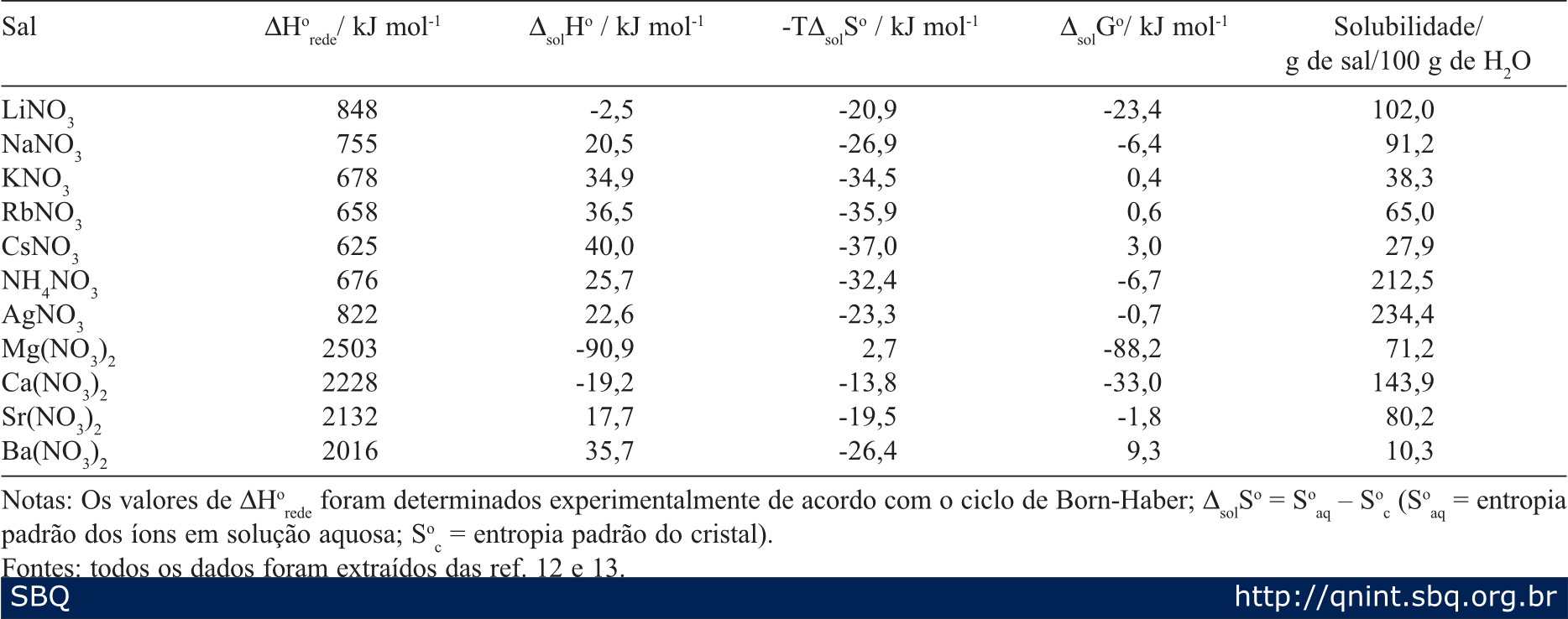
Toda a reação exotérmica é espontânea. A entropia é uma medida da energia que não pode ser convertida em trabalho. Resumindo: a entalpia estuda a energia total de um sistema, enquanto que a entropia estuda a energia que não pode ser transformada em trabalho ( energia dissipada). Seja o valor absoluto (módulo) deste calor. Se nos processos espontâneos há diminuição da energia e um aumento da entropia , podemos concluir que a entropia total do Universo tende a aumentar cada vez mais.
O que significa que a energia do Universo caminha em direção à desordem. Logo, cada vez menos energia poderá ser transformada em trabalho. Sº= a variação de entropia é uma função de estado que informa a variação de energia em função do estado de liberdade das partículas. Essa função é uma das mais usadas na química e na bioquímica em virtude desta. Assim, a produção do ATP nas pilhas armazena a energia livre de Gibbs que pode então ser usada para outros processos com a ajuda da reacção reversa que converte o ATP ao ADP e, no processo.
Segunda Lei da Termodinâmica e que tende a aumentar naturalmente no Universo. A grandeza da energia livre só é usada para calcular variações que ocorrem nos sistemas, e não para sistemas estáticos. Entalpia (representada pela letra “H”) é o nome atribuído à energia que fica armazenada nas substâncias ( energia interna), a espera que sofra alguma transformação para que seja alterada ou liberada. Na termodinâmica, a energia livre de Helmholtz é um potencial termodinâmico que mede a quantidade de energia disponível e extratível de um sistema fechado a temperatura e volume constantes. Usar valores tabelados de energia livre de formação, ∆Gfo.
Nesta situao o sistema tenta conseguir a maior estabilidade possvel, ou seja, a menor energia livre de Gibbs. La entropía es una función de estado de carácter extensivo. A velocidade da reação direta é rápida. A reação não é espontânea. A energia de Gibbs de uma fase estequiométrica apenas pode ser obtida através de dados calorimétricos.
De acordo com a definição de G (ver equação 56), entalpia e entropia devem ser conhecidas para uma dada condição de temperatura e pressão. Energia de Gibbs de fases estequiométricas. Podemos todavia determinar as variações sofridas por um sistema quando se passa de um. Portanto, a energia livre padrão é dada a uma temperatura de 298K e uma pressão de atm, mas o valor de energia livre pode variar dependendo da temperatura e pressão.
Vimos também que os sistemas químicos podem variar de um estado de alta energia para um de baixa energia , esta variação de energia é representada por ∆H. La energía libre o entalpía libre de Gibbs se emplea en química para explicar si una reacción sucederá de manera espontánea o no. Para calcular la energía libre de Gibbs se puede fundamentar en: el aumento o la disminución de la entropía asociada con la reacción, y la suma de calor requerida o liberada por la misma. El concepto de entropía desarrollado en respuesta a la observación de que una cierta cantidad de energía liberada de funcionales reacciones de combustión siempre se pierde debido a la disipación o la fricción y por lo tanto no se transforma en trabajo útil.
Josiah Willard Gibbs es, muy posiblemente, un nombre que no dirá nada a nadie. O Mercado Livre de energia é um ambiente de contratação de energia elétrica onde consumidores podem compram energia diretamente dos geradores ou comercializadores, através de contratos bilaterais com condições livremente negociadas, como preço, prazo, volume, etc.