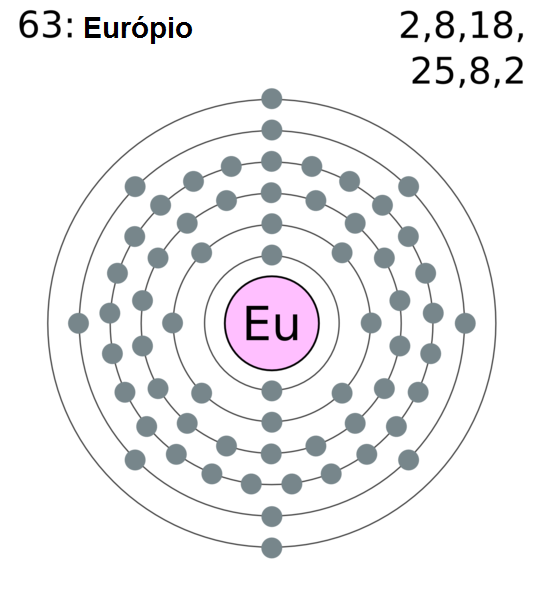
Por que o átomo possui essa tendência de realizar ligações químicas? E por que determinados átomos se sentem mais atraídos em realizar ligações com átomos de certos elementos do que com outros? Bom, a ligação química se estabelece entre os elétrons da camada mais externa da eletrosfera (camada de valência).
Achar o átomo central (não pode ser H nem O). Escrever os oxigênios ao redor do átomo central. As ligações iônicas, geralmente estabelecida entre um metal e um ametal (não metal), formam os compostos iônicos: elementos sólidos, duros e quebradiços que apresentam alto pontos de fusão e ebulição, além de conduzirem corrente elétrica quando dissolvidas em água.
Alguns átomos são estáveis, ou seja, pouco reativos. Já outros não podem ficar isolados. Precisam se ligar a outros elementos. Toda ligação envolve o movimento de elétrons nas camadas mais externas dos átomos. Para saber mais sobre o cursinho pré-vestibular mais forte e completo para o Enem e principais vestibulares, que adota uma metodologia exclusiva com Estudo O. O propósito deste texto é abordar aspectos referentes às forças intramoleculares, isto é, referentes às ligações químicas.

Sem nenhuma dúvida, ainda hoje as forças que atuam entre átomos representam um dos aspectos mais intrigantes de todo o estudo da química. Read More
.png)