Aquecendo o gás no Estado por meio de uma chama, as moléculas se agitam pelo aumento da temperatura e, devido a sua alta energia cinética, empurram o pistão para cima fazendo aumentar o volume. Aprende en este artículo qué es en termodinámica un proceso isobárico y cuáles son algunas de sus aplicaciones reales. Qué es el Proceso Isobárico. El término isobárico se compone de dos partes: iso = igual y bárico = presión.
Un proceso isobárico es un desarrollo termodinámico en el cual la presión permanece de forma constante. Esto generalmente se obtiene al permitir que el volumen se expanda o contraiga de tal manera que neutralice cualquier cambio de presión que pueda causar la transferencia de calor. En termodinámica, un proceso isobárico es un cambio en el estado de una cierta cantidad de materia en la que la presión no cambia, pero sí una o más de sus variables de estado. El proceso isobárico, es un proceso térmico de presión constante. Este artículo utiliza la convención de signos químicos para el trabajo, donde.
Conociendo el calor suministrado a un gas que se expande en litros a un presion constante de atmosfera, calcularemos el incremento de energia interna ΔU, aplicando el primer principio de. La primera ley de la termodinámica, para este caso, queda expresada como sigue: = −,. The heat transferred to the system does work , but also changes the internal energy of the system. This article uses the chemistry sign convention for work, where positive work is work done on the system. A utilização direta desses princípios em motores de combustão interna ou.
Transformacion ISOBARICA Capacidad calorífica específica del proceso isobárico Para encontrar la capacidad de calor específico molar del gas involucrado, las siguientes ecuaciones se aplican a cualquier gas general que sea calóricamente perfecto. In an isobaric process and the ideal gas, part of heat added to the system will be used to do work and part of heat added will increase the internal energy. Isobaric Process – Heat and Energy. On a p-V diagram, the process occurs along a horizontal line (called an isobar) that has the equation p = constant. Let assume an isobaric heat addition in an ideal gas.
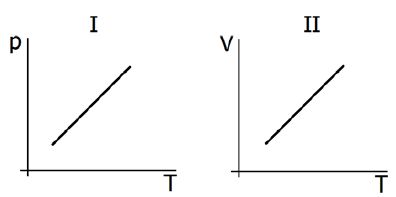
In an ideal gas, molecules have no volume and do not interact. Quanto ao comportamento da pressão e do volume, observe o exemplo no experimento a seguir (figura 1), cujo gás encerrado no interior do êmbolo é um gás perfeito. In termodinamica si definiscono isobare anche le linee che uniscono punti di uguale pressione, ovvero la rappresentazione di due o più condizioni caratterizzate da avere la stessa pressione. Le isobare sono dunque delle linee che agevolano la lettura delle trasformazioni termodinamiche in vari tipi di diagrammi.
En este caso parte del calor absorbido se transforma en trabajo realizado por el gas y el resto se invierte en aumentar la energía interna. La Ley de Charles, es una de las leyes de los gases. Relaciona el volumen y la temperatura de una cierta cantidad de gas ideal, mantenido a una presión constante, mediante una constante de proporcionalidad directa. Confira grátis, videos online de Transformação Isobárica de Leis da Termodinâmica para te ajudar em seus estudos para o Vestibular, ENEM, Reforço Escolar, Concursos e mais! In the isothermal process, the heat Q added (which tends to increase the temperature and internal energy) is exactly cancelled by the work W done by the gas on the surroundings (which tends to decrease the temperature and internal energy), so there is no change in internal energy or temperature of the gas.
Analogamente à transformação isotérmica, quando há uma transformação isobárica, a pressão é conservada. Qual a energia interna de mols de um gás perfeito na temperatura de 20°C? In questo formulario presentiamo tutte le formule della Termodinamica che si possono incontrare sia negli studi liceali che in quelli universitari. Alcune delle formule presentate in questo formulario si trovano in forma differenziale o in forma integrale per venire incontro alle necessità degli studenti universitari.

Uma massa m de ar, inicialmente a uma pressão de atm, ocupa m³ em um balão. Uma transformação isobárica é uma transformação termodinâmica na qual a pressão permanece constante em um sistema fechado, sistema este que permite trocas de energia, mas não de matéria, entre o sistema e sua vizinhança. Exercícios sobre a Primeira Lei da Termodinâmica para processos isobáricos Exercícios de Física Esta é uma lista de exercícios sobre a Primeira Lei da Termodinâmica para os processos isobáricos, isto é, quando a pressão é mantida constante.
PROCESO ADIABATICO : En termodinámica se designa como proceso adiabático a aquél en el cual el sistema (generalmente, un fluido que realiza un trabajo) no intercambia calor con su entorno. Resolva exercícios de vestibular sobre Termodinâmica, aprenda o passo-a-passo das resoluções e prepare-se: você vai gabaritar o Enem e os vestibulares! Haremos un ejercicio de QUIMICA de Bachiller, esta vez de TERMODINAMICA , transformaciones ISOBARICAS.
Otro ejemplo es la variación de volumen que experimenta una pelota conforme los rayos del sol indicen sobre ella. Al inicio de la mañana presenta cierta presión, volumen y temperatura, conforme se calienta el aire en su interior aumenta la presión, pero esta no varia debido al aumento de su volumen. En un diagrama P-V, un proceso isobárico aparece como una línea horizontal.
Proceso isotérmico es el cambio de temperatura reversible en un sistema termodinámico, siendo dicho cambio de temperatura constante en todo el sistema. Segunda Ley de la Termodinamica Estos son los códigos MathML y LaTeX de la fórmula. Gracias a ellos podrás integrarlas en cualquier programa externo compatible, ahorrándote la necesidad de escribirlas tu mismo desde cero.