Todo sistema tende a um equilíbrio térmico, que acontece depois de certo tempo. Agora imagina que o café ou o refrigerante já estivessem à mesma temperatura ambiente. Nesse caso, as temperaturas iriam permanecer iguais! Isto é: não haveria troca de calor. Nesta videoaula de Física sobre as leis da Termodinâmica, o kuadro retoma os conceitos de transferência de calor e apresenta o conceito de trabalho, uma outra forma de transferência de energia.
A termodinâmica se ocupa em geral com sistemas em equilíbrio. O vídeo apresenta uma introdução à primeira lei da termodinâmica, a conservação. Introdução às leis da termodinâmica 1. INTRODUÇÃO ÀS LEIS DA TERMODINÂMICA Teorias e conceitos 2. Para entrar como usuário e utilizar todos os recursos da Khan Academy, habilite o JavaScript em seu navegador. Os eventos do nosso dia-a-dia, como mudanças climáticas (correntes oceânicas, o vento, os fluxos de ar), atividades industriais (extração de metais, motores de combustão interna, refrigeradores, detonação de explosivos, etc.) podem ser analisados pelas chamadas três leis gerais da termodinâmica, que se. A variação da energia interna DU é medida pela diferença entre a quantidade de calor (Q), trocado pelo sistema com seu exterior, e o trabalho realizado (W) e é dada pela expressão DU = K – W , que corresponde ao enunciado da lei da termodinâmica.
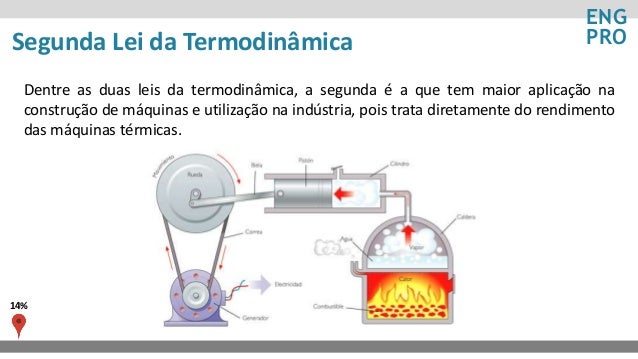
As leis fundamentais da termodinâmica regem o modo como o calor se transforma em trabalho e vice-versa. Primeira Lei da Termodinâmica. Isso quer dizer que a energia em um sistema não pode ser destruída nem criada, somente transformada. ESTRUTURA DA TEMODINÂMICA 1. O estudo desse ramo parte das Leis da Termodinâmica, leis essas que postulam que a energia pode ser transferida de um sistema para outro na forma de calor ou trabalho. A Termodinâmica Clássica não trata da evolução para equilíbrio: aceita-o e dele obtém relações entre grandezas mensuráveis sem fazer qualquer apelo à constituição atómica do sistema.
O corpo humano é um exemplo. A temperatura corporal permite-nos obter muitas informações importantes, incluindo o próprio estado de saúde. Afinal, o que é termodinâmica? A gente escuta bastante falar sobre termodinâmica e como ela é importante para a química, mas falta ainda uma definição, não é? Este blogue se destina a divulgar conhecimento, através dos livros. Baixe grátis o arquivo trabalho de fisica termodinamica TERMINADO.
Para uma introdução ao estudo da Termoquímica, veja como ela pode ser conceituada: A Termoquímica é um ramo da Físico-Química que estuda as reações químicas e os processos físicos que envolvem trocas de calor. Engenharia de Alimentos na UFMT. Essas reações e processos são extremamente importantes para a vida no planeta e também são muito frequentes no cotidiano.
Se você está vendo esta mensagem, significa que estamos tendo problemas para carregar recursos externos em nosso website. A introdução da segunda lei da termonâmica resolve esta inadequação da ocorrência de processos termodinâmicos. Pois, enquanto a primeira lei da termodinâmica estabelece a conservação de energia em qualquer transformação, a segunda lei estabelece condições para que as transformações termodinâmicas possam ocorrer.
Esta apostila foi criada com o intuito de desvendar a teoria da físico química de uma maneira diferente, dando grande importância aos conceitos e as leis. Segunda Lei da Termodinâmica Essa lei foi enunciada pelo físico francês Sadi Carnot, e estabelece restrições para a conversão de calor em trabalho, realizadas pelas máquinas térmicas. Termologia, Termodinâmica – 1ª Lei da Termodinâmica.

Chamamos de 1ª Lei da Termodinâmica o princípio da conservação de energia aplicada à termodinâmica, o que torna possível prever o comportamento de um sistema gasoso ao sofrer uma transformação termodinâmica. Na superfície da lua uma pessoa pesa cerca de um sexto do que normalmente pesaria na Terra Fig. A principal causa de confusão entre massa e peso é que a massa em geral é medida indiretamente calculando-se a força da gravidade exercida sobre ela, desconsiderando forças exercidas por outros efeitos, como o empuxo. A variação de energia livre (deltaG) depende da variação do conteúdo de calor (deltaH) e da variação no grau de desordem (deltaS) Energia livre de Gibbs, G: Quantidade de energia associada a uma reação, é a capacidade de realizar trabalho. Com este trabalho, realizado no âmbito da disciplina de Termodinâmica, consegui adquirir conhecimentos necessários e mais aprofundados sobre a matéria abordada, compressores, realizei este trabalho com dados retirados somente da internet.
Pelos princípios da hidrostática podemos concluir que, para uma diferença de nível, L em metros, em um manômetro em U, a diferença de pressão em Pascal é dada pela relação: ∆P = ρ gL. A Termodinâmica (do grego therme = calor e dynamis = movimento) é o ramo da Física que estuda os efeitos da mudança de temperatura, volume e pressão, empregados em sistemas físicos em escala macroscópica. De uma forma mais simples, a termodinâmica procura explicar os mecanismos de transferência de energia térmica a fim de que estes. Na verdade calor pode ser definido de várias formas diferentes.
NOTE: State license renewal information is provided as a convenience only and is subject to change at any time. It is the ultimate responsibility of the individual to be sure that he or she is meeting continuing education requirements for each license and corresponding renewal period. A fonte da energia solar são as reações de fusão nuclear entre núcleos de hidrogênio, resultando em núcleos de hélio mais uma certa quantidade da energia. O texto fornece uma cobertura completa dos princípios da termodinâmica e detalha as suas aplicações nos processos químicos. Da mesma forma que a temperatura Tse mantém constante durante o primeiro passo do ciclo de Carnot, a entropia SC = SB não varia na transformação adiabática de resfriamento desde a temperatura Tda fonte quente até a temperatura Tda fonte fria.
Portanto, o segundo passo do ciclo de Carnot é uma transformação isoentrópica.